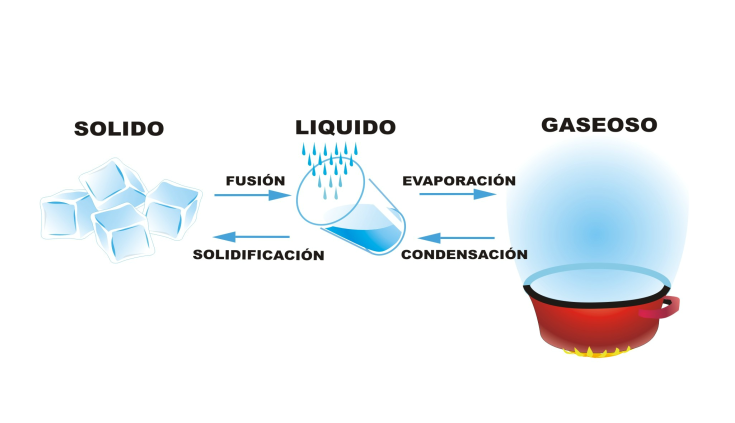
Los cambios de estado que se producen en la naturaleza tienen las siguientes características: son cambios reversibles, la temperatura permanece constante mientras dura el cambio de estado y la masa se conserva en el proceso, sin embargo, el volumen no siempre se conserva.

El estado de una sustancia depende de dos factores: naturaleza de la sustancia (de ella depende la fuerza de unión entre sus átomos) y temperatura (de ella depende la energía o rapidez con la que se mueven los átomos).
Un cuerpo en estado sólido al que se aumenta su temperatura hace que sus partículas se muevan más rápido hasta que se separan y pasa a estado líquido o gaseoso. Lo contrario pasa si se baja la temperatura, las partículas tendrán menos energía y tenderán a estar en estado líquido o sólido.
Para estudiar los cambios de estados se elaboró una teoría que plantea, que la materia está formada por partículas llamadas átomos o moléculas. Existen unas fuerzas de atracción que las mantienen mas o menos unidas. Estas partículas están en continuo movimiento, por eso la teoría se llama teoría cinética molecular.
¿Qué necesitamos para Cambiar de Estado?
En esta infografía que te mostramos, verás como se producen los cambios de estado de la materia cuando se va calentando un sólido (aumentando su temperatura), pasando a estado líquido y después a gas y qué sucede cuando se alcanzan los puntos de fusión y ebullición.
Conseguiremos un cambio de estado, si somos capaces de debilitar o aumentar la fuerza de unión de las partículas y/o aumentar o disminuir su movimiento.
Si está en estado sólido y conseguimos que se debilite la fuerza de unión entre sus partícula, llegará un momento que se convertirá en líquido, si se sigue debilitando, hasta que no haya fuerza de unión, pasará a estado gaseoso. El proceso es reversible. Pero…. ¿Cómo conseguimos esto?. Cambiando la Presión y/o la Temperatura de la sustancia. El estado de una sustancia está determinado por su temperatura y por la presión a la que se encuentra.
Por ejemplo, si pasamos de líquido a gas se llamará vaporización. si cambiamos de sólido a líquido se llamará fusión y al revés solidificación. fíjate en la dirección de la flecha para tener claro cada cambio de estado.

¿Y donde esta la ebullición?
En la vaporización, paso de líquido a gas, existen dos tipos diferentes, o dos formas de hacer el cambio de estado: ebullición y evaporación.
Ebullición: cuando el cambio de estado se produce de forma rápida. En este caso se hace llegando a la temperatura de ebullición, por ejemplo el agua es de 100ºC. Este agua pasará de estado líquido a sólido rápidamente.
Vaporización: cuando el cambio de estado se produce de forma lenta. Si dejamos un vaso de agua en la ventana, al cabo de un tiempo este agua se evapora, es decir pasa de líquido a gas, pero el proceso lo ha realizado lentamente, sin llegar a la temperatura llamada de ebullición. Para este caso no es necesario que lleguemos a la temperatura de ebullición de la sustancia.
Mediante la siguiente infografía, podrás comprender cómo se producen los cambios de estado en un sólido, líquido o gas, en cuanto a la energía y al movimiento de las partículas, tomando como ejemplo el agua En la simulación debes aumentar o disminuir la temperatura del agua.
Los cambios de estado se hacen suministrando calor o frío. Cada materia tiene un punto de ebullición y fusión diferentes. Veamos ahora los diferentes puntos (temperaturas) a los que diferentes tipos de materia cambian de estado:
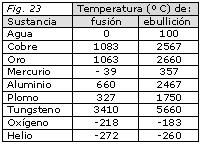
Como vemos cada tipo de materia diferente tiene sus propios puntos de fusión y ebullición y son exclusivos de ella. Si tenemos una caja con un tipo de materia y para averiguar cuál es damos una pista, su punto de fusión es de -39ºC. ¿Cual sería? Pues solo podría ser el Mercurio.
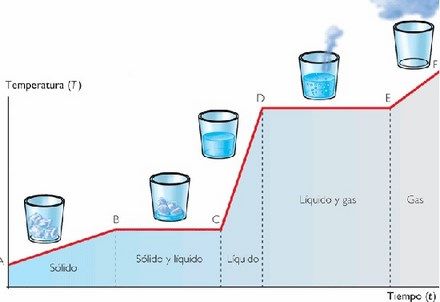
El punto D sería para 100ºC en el caso del agua. Fíjate que durante un tiempo suministramos calor al agua a 100ºC para que pase todo el líquido a gas (desde D hasta E). Conviven en los dos estados. En el punto E ya tenemos todo el líquido convertido en gas.
Lo mismo ocurre para pasar de líquido a sólido a 0ºC. Empezaría la conversión en el punto C (0ºC) y en B ya tendríamos todo el líquido en estado sólido.
Con este video que te presentamos a acontinuación, podrás reforzar los conocimientos adquiridos anteriormente.
La siguiente simulación tomada de phet.colorado.edu/, puedes utilizarla para poner tus estudiantes a ver los diferentes estados de la materia
Descripción
Mira los diferentes tipos de moléculas que forman un sólido, líquido o gas. Agrega o elimina el calor y ve el cambio de fase. Cambia la temperatura o el volumen de un contenedor y ve un diagrama de presión-temperatura responder en tiempo real. Relacionar el potencial de interacción de las fuerzas entre las moléculas.
Objetivos de aprendizaje de la muestra
- Describir un modelo molecular para sólidos, líquidos y gases.
- Extender este modelo a los cambios de fase.
- Describir cómo la calefacción o refrigeración cambia el comportamiento de las moléculas.
- Describir cómo cambiando el volumen puede afectar a la temperatura, presión y estado.
- Relacionar un diagrama de presión-temperatura en el comportamiento de las moléculas.
Enlaces relacionados
Fuentes